Agonisty GLP1-receptorov: antidiabetiká s antiaterogénnym účinkom
GLP-1 receptor agonists: antidiabetic agents with antiatherogenic effect
GLP-1 receptor agonists (GLP1 RA) have been used in the treatment of type 2 diabetes for the past 15 years. In the last five years, several randomized clinical trials with drugs of this group – liraglutide, semaglutide, albiglutide and dulaglutide – have demonstrated their ability to prevent major cardiovascular events. Therefore, some international recommendations list them as the drugs of the first choice in the treatment of patients with type 2 diabetes and proven clinical or subclinical atherosclerosis.
Keywords:
cardiovascular prevention – GLP-1 receptor agonists – treatment of type 2 diabetes
Autoři:
Ivan Tkáč
Působiště autorů:
Excelentný tím pre výskum aterosklerózy (EXTASY), IV. interná klinika UPJŠ LF a UN LP Košice
Vyšlo v časopise:
AtheroRev 2020; 5(3): 181-184
Kategorie:
Klinická studie
Souhrn
Agonisty GLP1-receptorov (GLP1 RA) sa používajú na liečbu diabetu 2. typu počas posledných 15 rokov. V posledných 5 rokoch viaceré klinické randomizované štúdie s preparátmi tejto skupiny – liraglutidom, semaglutidom, albiglutidom a dulaglutidom – preukázali ich schopnosť prevencie závažných kardiovaskulárnych príhod. Preto niektoré medzinárodné odporúčania ich uvádzajú ako lieky prvej voľby pri liečbe pacientov s diabetom 2. typu a preukázanou klinickou či subklinickou aterosklerózou.
Klíčová slova:
agonisty GLP1-receptorov – kardiovaskulárna prevencia – liečba diabetes mellitus 2. typu
Úvod – antidiabetiká a prevencia kardiovaskulárnych príhod
Liečba ochorenia diabetes mellitus 2. typu (DM2T) zaznamenala v posledných 15 rokoch nebývalý pokrok. Po desaťročia boli k dispozícii na liečbu DM2T iba deriváty sulfonylurey, bigvanidy a inzulín, prípadne akarbóza. Spomedzi týchto liekov bol pozorovaný efekt na prevenciu kardiovaskulárnych príhod len pri liečbe metformínom u novodiagnostikovaných diabetikov 2. typu [1]. Koncom minulého storočia a v prvej dekáde tohto storočia sa veľké nádeje vkladali do novej skupiny antidiabetík – glitazónov. Pioglitazón bol efektívny v prevencii závažných kardiovaskulárnych príhod [2]. Roziglitazón podľa výsledkov metaanalýzy včasných štúdií viedol k zvýšenému výskytu závažných kardiovaskulárnych príhod, a preto bola jeho registrácia v Európskej únii zrušená [3], aj keď neskoršie štúdia RECORD nepotvrdila zvýšenie incidencie kardiovaskulárnych príhod pri liečbe roziglitazónom [4]. Vzhľadom na bezpečnostné signály pozorované pri roziglitazóne nariadili regulačné inštitúcie vykonanie štúdií kardiovaskulárnej bezpečnosti pre všetky antidiabetiká uvedené do klinickej praxe.
Výsledky týchto štúdií boli publikované od roku 2013 a 2 skupiny nových antidiabetík – inhibítory sodíkoglukózového kotransportéru 2 (SGLT2i) a agonisty receptorov glukagónu podobného peptidu 1 (GLP1 RA), dokázali okrem kardiovaskulárnej bezpečnosti aj efekt na prevenciu závažných kardiovaskulárnych príhod.
SGLT2i znižujú kardiovaskulárnu morbiditu a mortalitu prostredníctvom hemodynamických efektov, hlavne svojím účinkom na zlyhávanie srdca a pravdepodobne aj na progresiu chronického ochorenia obličiek [5].
Skupine GLP1 RA sa budeme venovať v nasledujúcom prehľade.
Mechanizmus antidiabetického účinku GLP1 RA
Sekrécia inzulínu z B-buniek je regulovaná viacerými mechanizmami, z ktorých sú najdôležitejšie dva. Ak vzrastie hladina glykémie, glukóza vstupuje do B-buniek Langerhansových ostrovčekov prostredníctvom glukózového transportéra 2 (GLUT2) a následne sa spúšťa reťaz metabolických dejov vedúcich k glukózou stimulovanej sekrécii inzulínu. Ďalším mechanizmom spúšťanie sekrécie inzulínu je inkretínový efekt. Pri príjme zmiešanej stravy a jej vstupe do tenkého čreva dochádza k sekrécii inkretínov – GLP1 a glukózodependentného inzulinotropného peptidu (GIP). Tieto stimulujú sekréciu inzulínu z B-buniek pankreasu mechanizmom nezávislým od glukózy cez svoje špecifické receptory. GLP1 je zodpovedný za väčšinu účinku na inzulínovú sekréciu. V natívnej forme však nie je možné jeho použitie, nakoľko je v priebehu minút degradovaný enzýmom dipeptidylpeptidáza-4 (DPP4). Vzhľadom na to boli vyvinuté 2 farmakologické prístupy využiteľné v liečbe diabetu. Perorálna inhibícia DPP4 vedie k reštaurácii fyziologických hladín GLP1 a GIP [6]. Inhibítory DPP4 v štúdiách kardiovaskulárnej bezpečnosti a prevencie síce dokázali svoju bezpečnosť, ale nie schopnosť znížiť počet závažných kardiovaskulárnych príhod [7]. Na rozdiel od nich GLP1 RA viedli v 6 zo 7 ukončených štúdií k redukcii aspoň 1 kardiovaskulárneho výsledku [8–14].
Prehľad štúdií s GLP1 RA pri DM2T
V roku 2015 boli publikované výsledky prvej štúdie kardiovaskulárnej bezpečnosti zo skupiny GLP1 RA s lixisenatidom (ELIXA). Štúdia bola vykonaná na vysoko rizikovej populácii diabetikov, ktorí prekonali infarkt myokardu (IM) alebo boli hospitalizovaní pre nestabilnú anginu pectoris (NAP) v období 6 mesiacov pred randomizáciou. Primárnym kompozitným výsledkom štúdie bola mortalita z kardiovaskulárnych príčin (KVM), infarkt myokardu (IM), cievna mozgová príhoda (CMP) alebo NAP. Incidencia primárneho výsledku v placebovej skupine bola 63/1 000 pacient-rokov (PR). To ukazuje na extrémnu kardiovaskulárnu rizikovosť zaradených pacientov, keďže extrapolácia uvedenej incidencie by znamenala, že v priebehu 10 rokov dosiahne primárny výsledok až 63 % pacientov. Výskyt primárneho výsledku na 1 000 PR v placebovej skupine najpresnejšie vystihuje rizikovosť zaradených pacientov, keďže berie do úvahy okrem zastúpenia pacientov s predchádzajúcim kardiovaskulárnym alebo renálnym postihnutím aj ďalšie charakteristiky študovanej skupiny chorých (vek, pohlavie, prítomnosť ďalších rizikových faktorov). V ďalšom texte budeme preto uvádzať tento parameter ako hlavnú charakteristiku jednotlivých študijných populácií. Štúdia ELIXA síce potvrdila kardiovaskulárnu bezpečnosť lixisenatidu, ale nepotvrdila jeho superioritu voči placebu [8].
Výsledky štúdie s lixisenatidom boli v zhode s publikovanými štúdiami s inhibítormi DPP4, ktoré tiež potvrdili kardiovaskulárnu bezpečnosť tejto skupiny liekov, ale nie kardioprotektivitu [7]. V roku 2016 v priebehu niekoľkých mesiacov hneď 2 štúdie s GLP1 RA ukázali potenciál agonizmu GLP1-receptorov znížiť výskyt závažných kardiovaskulárnych príhod. V prvej z týchto štúdií bol sledovaný efekt liraglutidu (LEADER) ako prídavnej liečby v porovnaní s placebom. Medián trvania štúdie bol 3,8 roka. Primárny kompozitným kardiovaskulárnym výsledkom v tejto a ďalších nižšie uvedených štúdiách bolo úmrtie z kardiovaskulárnych príčin, incidencia nefatálneho IM alebo nefatálnej CMP. Incidencia primárneho výsledku v placebovej skupine bola 39/1 000 PR.
V skupine, ktorá dostávala liraglutid, bola zistená signifikantná redukcia primárneho výsledku o 13 % (p = 0,01). Mortalita z kardiovaskulárnych príčin bola tiež signifikantne znížená o 22 % (p = 0,007), zatiaľ čo celková mortalita bola nižšia o 15 % (p = 0,02). Navyše bolo pozorované aj signifikantné zníženie incidencie fatálneho a nefatálneho IM o 14 % (p = 0,046) [9].
Kým lixisenatid a liraglutid sa podávajú subkutánne 1-krát denne, ďalšie štúdie sledovali efekt GLP1 RA podávaných subkutánne 1-krát týždenne.
Prvá publikovaná štúdia s GLP1 RA podávaným 1-krát týždenne (SUSTAIN-6) sledovala efekt semaglutidu. Do štúdie boli zaradení diabetici starší ako 50 rokov s dokázaným kardiovaskulárnym ochorením alebo s chronickým obličkovým ochorením štádia 3. Pokiaľ boli pacienti starší ako 60 rokov, postačovala na zaradenie prítomnosť aspoň jedného ďalšieho kardiovaskulárneho rizikového faktora. Rizikovosť pacientov zaradených do štúdie bola podobná ako v štúdii s liraglutidom, keď incidencia rovnako definovaného primárneho kompozitného výsledku v placebovej skupine bola 44/1 000 PR. Medián trvania štúdie bol 1,9 roka. Za toto obdobie bolo pri liečbe semaglutidom pozorované zníženie primárneho výsledku o 26 % (p = 0,02). Zo zložiek primárneho výsledku bola signifikantne znížená incidencia nefatálnej CMP o 39 % (p = 0,04) [10].
Exenatid bol prvý GLP1 RA používaný v klinickej praxi, pričom bolo potrebné subkutánne dávkovanie 2-krát denne. Neskôr vyvinutý depotný exenatid QW pre užívanie 1-krát týždenne bol testovaný v štúdii kardiovaskulárnej bezpečnosti (EXSCEL). 73 % pacientov malo predchádzajúce kardiovaskulárne ochorenie, čo zodpovedalo incidencii primárneho kompozitného výsledku 40/1 000 PR v placebovej skupine. Medián sledovania pacientov v štúdii bol 3,2 roka.
V skupine liečenej exenatidom bolo pozorované zníženie primárneho kardiovaskulárneho výsledku o 9 %, čo bolo na hranici štatistickej významnosti (p = 0,06). Žiadna zo zložiek primárneho výsledku nebola signifikantne znížená v intervenčnej skupine, ale bolo pozorované signifikantné zníženie celkovej mortality v skupine liečenej exenatidom o 13 % (95% CI: 23–3 %) [11].
V ďalšej štúdii bol sledovaný efekt prídavnej liečby albiglutidom podávaným subkutánne 1-krát týždenne v porovnaní s placebom. Rizikovosť pacientov bola podobne extrémne vysoká ako v štúdii s lixisenatidom, v ktorej mali všetci pacienti zaradení do štúdie predchádzajúce kardiovaskulárne ochorenia a incidencia primárneho výsledku v placebovej skupine bola 59/1 000 PR. Pri mediáne trvanie štúdie 1,5 roka viedla prídavná liečba albiglutidom k signifikantnej redukcii incidencie primárneho výsledku o 22 % (p = 0,0006). Okrem toho bolo pozorované signifikantné zníženie incidencie fatálneho a nefatálneho infarktu myokardu o 15 % (p = 0,003) [12].
V poradí posledná ukončená štúdia so subkutánne aplikovaným GLP1 RA (REWIND) testovala efekt dulaglutidu podávaného 1-krát týždenne v najmenej rizikovej populácii pacientov s DM2T. Incidencia primárneho kardiovaskulárneho výsledku v kontrolnej skupine bola 27/1 000 PR a medián trvania štúdie bol 5,4 roka. Prídavná liečba dulaglutidom viedla k signifikantnému zníženiu incidencie primárneho výsledku o 12 % (p = 0,026) v porovnaní s placebom. Incidencia nefatálnej CMP bola tiež signifikantne nižšia o 24 % (p = 0,017) [13].
Prvá štúdia s perorálne aplikovaným semaglutidom (PIONEER 6) priniesla ďalšie povzbudivé výsledky. Aj keď v tejto štúdii nebola pozorovaná signifikantná redukcia primárneho výsledku pri prídavnej liečbe semaglutidom (HR 0,79; 95% CI 0,57–1,11), 2 dôležité sekundárne výsledky boli signifikantne ovplyvnené liečbou semaglutidom. V porovnaní s kontrolnou skupinou bolo pozorované zníženie ako kardiovaskulárnej (HR 0,49; 95% CI 0,27–0,92), tak aj celkovej mortality (HR 0,51; 95% CI 0,31–0,84) o polovicu [14].
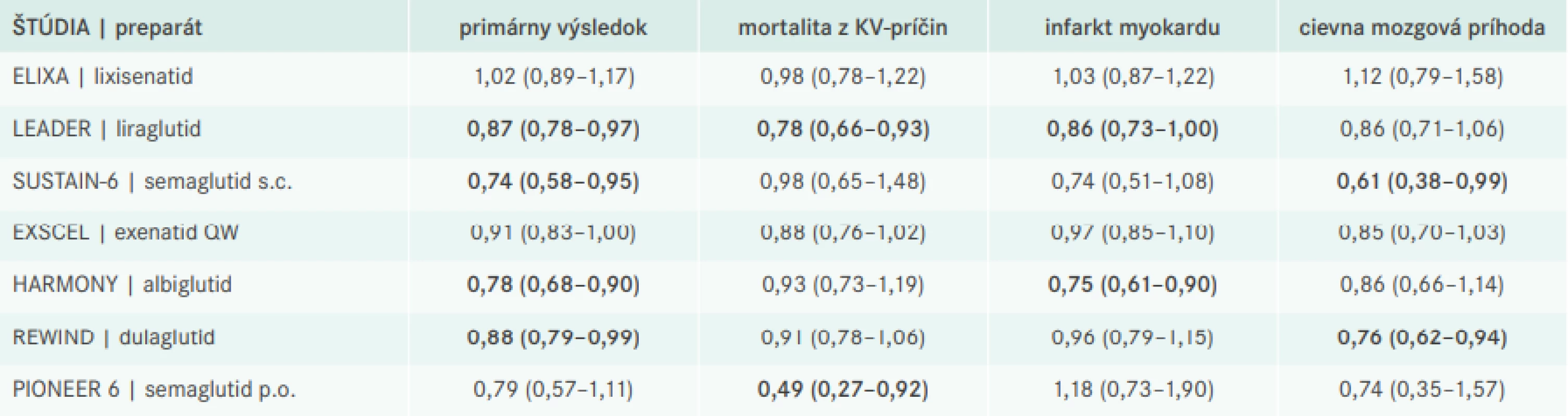
Prehľad výsledkov štúdií s GLP1 RA je zhrnutý v tab. V súhrne možno konštatovať, že signifikantné zníženie primárneho výsledku bolo pozorované v štúdiách s liraglutidom, semaglutidom, albiglutidom a dulaglutidom. Navyše zníženie kardiovaskulárnej mortality bolo pozorované v štúdiách s liraglutidom a perorálne podávaným semaglutidom, zatiaľ čo zníženie incidencie IM v štúdiách s liraglutidom a albiglutidom a zníženie incidencie CMP v štúdiách s liraglutidom a dulaglutidom. Celková mortalita bola redukovaná v štúdiách s liraglutidom, perorálne podávaným semaglutidom a exenatidom QW. Metaanalýza všetkých uvedených štúdií ukázala signifikantné zníženie všetkých sledovaných kardiovaskulárnych výsledkov [14]. Takýto dôkaz z metaanalýzy svedčí o efektivite mechanizmu aktivácie GLP1-receptorov v prevencii kardiovaskulárnych príhod, ale nie o efektivite jednotlivých preparátov z danej skupiny liekov, ktoré sa posudzujú na základe výsledkov individuálnych štúdií. Ideálny prípad je, keď pozitívny efekt jednotlivého lieku je replikovaný v ďalšej štúdii. Takýto replikačný dôkaz má iba semaglutid, aj keď len parciálny, nakoľko máme k dispozícii výsledky 2 štúdií, pričom v jednej z nich bol semaglutid podávaný subkutánne 1-krát týždenne a v druhej perorálne 1-krát denne [10,14].
Z vedľajších účinkov liečby GLP1 RA je potrebné spomenúť gastrointestinálnu intoleranciu (nauzea, zvracanie, hnačky), ktorá je zvyčajne prechodná, aj keď asi v 10–15 % prípadov môže viesť k včasnému vysadeniu liečby [8–14]. Táto súvisí s tlmivým účinkom aktivácie GLP1-receptorov na motilitu gastrointestinálneho traktu. Tento účinok v žlčníku a žlčových cestách je pravdepodobne zodpovedný aj za vyšší výskyt cholelitiázy a akútnej cholecystitídy pozorovaný v niektorých štúdiách s GLP1 RA [9,12]. Prekvapujúcim nežiadúcim účinkom liečby bola častejšia progresia diabetickej retinopatie, ktorá bola signifikantne častejšia v štúdii so subkutánne podávaným semaglutidom v porovnaní s placebom [10]. Retrospektívny pohľad na túto komplikáciu ukázal, že podobný trend bol pozorovaný aj v štúdiách s liraglutidom a dulaglutidom, čo pravdepodobne súvisí s aktiváciou GLP1-receptorov v retinálnych cievach [9,13]. Pred začatím liečby GLP1 RA je preto vhodné vykonať vyšetrenie očného pozadia. U diabetikov s proliferatívnou retinopatiou a/alebo edémom makuly je liečba týmito preparátmi nevhodná.
Mechanizmus kardiovaskulárnej protekcie GLP1 RA
Tento mechanizmus nie je zatiaľ celkom objasnený, ale zdá sa, že GLP1 RA ovplyvňujú proces progresie aterosklerózy pleiotropne. Štúdie na humánnych subjektoch ukázali, že GLP1 RA okrem ovplyvnenia glykémie pozitívne ovplyvňujú aj ďalšie rizikové faktory aterosklerózy obzvlášť obezitu a hypertenziu. Štúdie na experimentálnych zvieratách ukázali pozitívne efekty na viacerých úrovniach rozvoja aterogenézy od priaznivého ovplyvnenia funkcie endotelu, zníženia zápalového procesu v cievnej stene až po zníženú aktiváciu trombocytov [16]. Toto naznačuje vhodnosť ich podávania už vo včasných štádiách diabetu, v ktorých je proces aterosklerózy menej rozvinutý a často skrytý bežným diagnostickým testom. Posledné spoločné odporúčania ADA/EASD uvádzajú GLP1 RA dokonca ako lieky prvej voľby u diabetikov 2. typu s klinickými, ale aj subklinickými prejavmi aterosklerózy koronárnych, cerebrálnych a periférnych tepien, ako aj u pacientov s chronickým obličkovým ochorením 3. štádia [17].
prof. MUDr. Ivan Tkáč, PhD. | ivan.tkac@upjs.sk | www.upjs.sk/vyskum/vedeckovyskumna-cinnost/spickove-timy/extasy-tim
Doručené do redakcie | Doručeno do redakce | Received 26. 8. 2020
Zdroje
- Effect of intensive blood-glucose control with metformin on complications in overweight patients with type 2 diabetes (UKPDS 34). UK Prospective Diabetes Study (UKPDS) Group. Lancet 1998; 352(9131): 854–865. Erratum in Lancet 1998; 352(9139): 1558.
- Dormandy JA, Charbonnel B, Eckland DJ et al. Secondary prevention of macrovascular events in patients with type 2 diabetes in the PROactive Study (PROspective pioglitAzone Clinical Trial In macroVascular Events): a randomised controlled trial. Lancet 2005; 366(9493): 1279–1289. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(05)67528–9>.
- Nissen SE, Wolski K. Effect of rosiglitazone on the risk of myocardial infarction and death from cardiovascular disease. N Engl J Med 2007; 356(24): 2457–2471. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa072761>.
- Home PD, Pocock SJ, Beck-Nielsen H et al. [RECORD Study Team]. Rosiglitazone evaluated for cardiovascular outcomes in oral agent combination therapy for type 2 diabetes (RECORD): a multicentre, randomised, open-label trial. Lancet 2009; 373(9681): 2125–2135. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(09)60953–3>.
- Verma S, McMurray JJ. SGLT2 inhibitors and mechanism of cardiovascular benefit: a state-of-the-art review. Diabetologia 2018; 61(10): 2108–2117. Dostupné z DOI: <http://dx.doi.org/10.1007/s00125–018–4670–7>.
- Nauck MA, Meier JJ. Incretin hormones. Their role in health and disease. Diabetes Obes Metab 2018; 20(Suppl 1): S5-S21. Dostupné z DOI: <http://dx.doi.org/10.1111/dom.13129>.
- Home P. Cardiovascular outcome trials of glucose-lowering medications: an update. Diabetologia 2019; 62(3): 357–369. Dostupné z DOI: <http://dx.doi.org/10.1007/s00125–018–4801–1>.
- Pfeffer MA, Claggett B, Diaz R et al. Lixisenatide in patients with type 2 diabetes and acute coronary syndrome. N Engl J Med 2015; 373(23): 2247–2257. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1509225>.
- Marso SP, Daniels GH, Brown-Frandsen K et al. Liraglutide and cardiovascular outcomes in type 2 diabetes. N Engl J Med 2016; 375(4): 311–322. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1603827>.
- Marso SP, Bain SC, Consoli A et al. Semaglutide and cardiovascular outcomes in patients with type 2 diabetes. N Engl J Med 2016; 375(19): 1834–1844. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1607141>.
- Holman RR, Bethel MB, Mentz RJ et al. Effects of once-weekly exenatide on cardiovascular outcomes in type 2 diabetes. N Engl J Med 2017; 377 : 1228–1239. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1612917>.
- Hernandez AF, Green JB, Janmohamed S et al. Albiglutide and cardiovascular outcomes in patients with type 2 diabetes and cardiovascular disease (Harmony Outcomes): a double-blind, randomised placebo-controlled trial. Lancet 2018; 392(10157): 1519–1529. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(18)32261-X>.
- Gerstein HC, Calhoun HM, Dagenais GR et al. Dulaglutide and cardiovascular outcomes in type 2 diabetes (REWIND): a double-blind, randomised placebo-controlled trial. Lancet 2019; 394(10193): 121–130. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(19)31149–3>.
- Husain M, Birkenfeld A, Donsmark M et al. Oral semaglutide and cardiovascular outcomes in patients with type 2 diabetes. N Engl J Med 2019; 381 : 841–851. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1901118>.
- Drucker DJ. The ascending GLP-1 road from clinical safety to reduction of cardiovascular complications. Diabetes 2018; 67(9): 1710–1719. Dostupné z DOI: Dostupné z DOI: <http://dx.doi.org/10.2337/dbi18–0008>.
- Kristensen SL, Rørth R, Jhund PS et al. Cardiovascular, mortality, and kidney outcomes with GLP-1 receptor agonists in patients with type 2 diabetes: a systematic review and meta-analysis of cardiovascular outcome trials. Lancets Diabetes Endocrinol 2019; 7(10):776–785. Dostupné z DOI: <http://dx.doi.org/10.1016/S2213–8587(19)30249–9>.
- Buse JB, Wexler DJ, Tsapas A et al. 2019 update to: Management of hyperglycaemia in type 2 diabetes, 2018. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetologia 2020; 63(2): 221–228. Dostupné z DOI: <http://dx.doi.org/10.1007/s00125–019–05039-w>.
Štítky
Angiologie Diabetologie Interní lékařství Kardiologie Praktické lékařství pro dospěléČlánek vyšel v časopise
Athero Review

2020 Číslo 3
-
Všechny články tohoto čísla
- Editorial
- Genetické testování familiární hypercholesterolemie v klinické praxi: stanovisko výboru České společnosti pro aterosklerózu
- Vplyv inhibítorov SGLT2 na aterosklerózu a reálna prax
- Hypertriglyceridemie – současnost a budoucnost
- Vybrané biomarkery asociované s aterosklerózou aj metabolizmom kostí
- Variabilita pacientů v nutričních kazuistikách
- Mendelovské randomizační studie: princip a příklady využití v oblasti kardiovaskulární medicíny
- Agonisty GLP1-receptorov: antidiabetiká s antiaterogénnym účinkom
- LIPIcontrol 2 aneb co se změnilo po 3 letech
- Novinky v liečbe evolokumabom: komentár k štúdiam VESALIUS-CV a FOURIER
- Novinky v liečbe alirokumabom prezentované na kongrese European Society of Cardiology 2020: komentár k post-hoc analýze štúdie ODYSSEY OUTCOMES
- Malá změna úhrad znamená velkou šanci pro mnoho nemocných
- Rešerše zajímavých článků ze zahraniční literatury
- Profesor Rudolf Poledne osmdesátiletý
- Šobrův den 2020: XXXIV. konference o hyperlipoproteinemiích tentokrát virtuálně
- Athero Review
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Hypertriglyceridemie – současnost a budoucnost
- Genetické testování familiární hypercholesterolemie v klinické praxi: stanovisko výboru České společnosti pro aterosklerózu
- Agonisty GLP1-receptorov: antidiabetiká s antiaterogénnym účinkom
- Mendelovské randomizační studie: princip a příklady využití v oblasti kardiovaskulární medicíny
